¿Qué es la enfermedad de Alzheimer?
La demencia, también denominada trastorno neurocognitivo mayor, engloba un conjunto de síntomas concurrentes cuyo síntoma principal es el deterioro cognitivo severo que afecta al funcionamiento y a las actividades de la vida diaria de las personas que la padecen.
La enfermedad de Alzheimer es la forma más común de demencia (entre el 60-80% de los casos). Se considera una enfermedad neurocognitiva del envejecimiento, ya que su prevalencia en poblaciones occidentales aumenta desde un 1% entre los individuos de 65 años hasta un 25% entre los individuos mayores de 90 años. Dado el continuo envejecimiento de la población, la enfermedad de Alzheimer ha sido catalogada como la epidemia del siglo XXI, siendo una de las principales prioridades a nivel de salud pública.
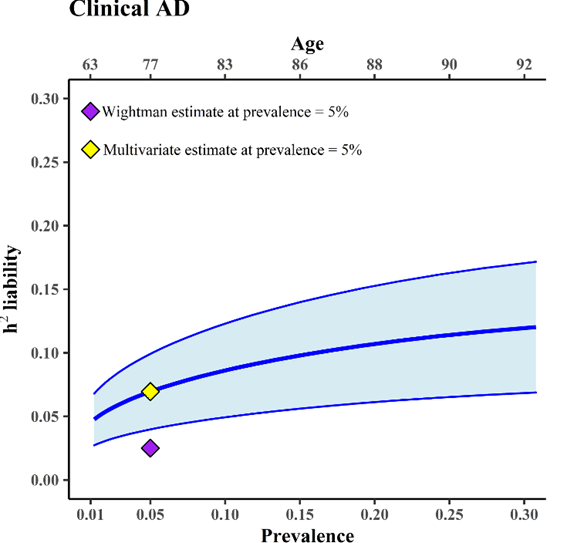
A nivel cognitivo, la enfermedad de Alzheimer se caracteriza por problemas en la memoria, dificultades para reconocer o recordar los nombres de las cosas (anomia), problemas de orientación, deterioro en la capacidad de razonamiento y toma de decisiones. Los síntomas al inicio de la enfermedad son sutiles y empeoran progresivamente hasta el punto de interferir con las tareas cotidianas. Por tanto, los déficits cognitivos de la enfermedad de Alzheimer varían en función de la etapa de la enfermedad en la que nos encontremos:
- Síntomas de enfermedad de Alzheimer leve: es la etapa temprana y leve de la enfermedad de Alzheimer. La persona es capaz de desenvolverse de forma independiente. No obstante, la persona presenta episodios de pérdida de memoria leves o incluso de la ubicación de objetos que utiliza en el día a día.
- Síntomas de enfermedad de Alzheimer moderado: se trata de la etapa moderada y más larga de la enfermedad de Alzheimer. La persona tiene dificultades para expresar sus pensamientos y realizar tareas cotidianas. Empiezan las confusiones de lugares, fechas, nombres, información personal como el número de teléfono, desorientación, cambio en los patrones de sueño, problemas para controlar la necesidad de ir al baño…
- Síntomas de enfermedad de Alzheimer severo: se trata de la etapa más grave. La comunicación se vuelve muy costosa, se experimentan cambios en las capacidades físicas, incluida la capacidad de hablar, sentarse y, eventualmente, tragar. La persona no es capaz de desenvolverse por sí sola y pierde la noción de experiencias recientes, recuerdos y hechos que le rodean.

Arquitectura genética de la enfermedad de Alzheimer
Desde un punto de vista genético, el Alzheimer puede dividirse en dos subgrupos:
- Casos de aparición tardía o esporádicos: se trata del subgrupo más común (90-95% de los casos) influenciado por múltiples variantes comunes cuyo efecto individual en la enfermedad es bajo. La heredabilidad (proporción de variación de un rasgo en una población que se puede atribuir a factores genéticos) se encuentra entre el 70-80% y su análisis es posible con un genotipado (tecnología genómica usada en los test de adn de ADNTRO).
- Casos de inicio temprano o familiar: se trata de un Alzheimer de aparición temprana poco frecuente (5-10% de los casos) que se da en personas menores de 65 años y la heredabilidad, en este caso, es entorno al 90%. Suele explicarse por variantes genéticas poco frecuentes que tienen un fuerte efecto sobre la enfermedad. Su análisis se lleva a cabo con la secuenciación del genoma completo (servicio disponible en ADNTRO).
Cuando hablamos de variantes genéticas y efectos, nos encontramos con la siguiente tendencia.
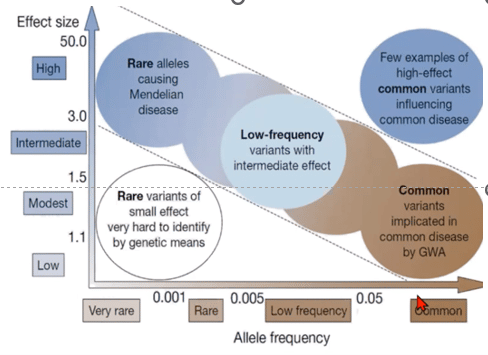
Existen variantes poco frecuentes que pueden causar la aparición temprana de la enfermedad de Alzheimer, por ejemplo: variantes poco frecuentes en los genes PSEN1, PSEN2 y APP. Por lo contrario, las variantes comunes (frecuentes en la población) por sí solas suelen influir menos en la enfermedad (el efecto es menor) haciendo necesaria la existencia de múltiples variantes comunes asociadas a dicha enfermedad para presentar una predisposición alta a desarrollarla.
En ADNTRO analizamos biomarcadores genéticos asociados con el Alzheimer de inicio tardío, analizando por tanto variantes genéticas comunes altamente asociadas con el Alzheimer.
Tu predisposición genética a desarrollar Alzheimer
En ADNTRO analizamos biomarcadores genéticos comunes asociados con la enfermedad de Alzheimer de inicio tardío, basados en descubrimientos de estudios de asociación del genoma (GWAS) de gran escala llevados a cabo en grandes biobancos.
Para calcular tu predisposición o protección frente a la enfermedad de Alzheimer nos basamos en un estudio científico reciente en el cual identifican más de dos mil variantes genéticas comunes asociadas con dicha enfermedad.
¡Conoce tu predisposición genética frente a la enfermedad de Alzheimer en ADNTRO!
Genética detrás de la enfermedad de Alzheimer
Las variantes genéticas de riesgo relacionadas con la enfermedad de Alzheimer incrementan el riesgo de desarrollar la enfermedad en términos probabilísticos, por lo que un riesgo genético alto para desarrollar la enfermedad de Alzheimer no significa que vayas a desarrollar la misma. Si bien es cierto que ser portador homocigótico del haplotipo APOE-ɛ4 se asocia con un riesgo de desarrollar la enfermedad de Alzheimer entre 8 y 10 veces mayor que los no portadores de dicha forma del gen (variación genética en dicho gen explica aproximadamente un 10% del riesgo genético para la enfermedad de Alzheimer).
Las variantes genéticas son puntos concretos del ADN y por tanto pertenecen o están muy próximas a ciertos genes.
Entre los genes más relevantes para la enfermedad de Alzheimer encontramos:
- CLU: ayuda a regular la eliminación de beta amiloide del cerebro.
- CR1: un déficit de la proteína codificada por este gen puede contribuir a la inflamación crónica del cerebro.
- PICALM: involucrado en la sinapsis. Una correcta sinapsis es fundamental para el funcionamiento adecuado de las neuronas y la formación de la memoria.
- APOE: es un gen altamente estudiado y relacionado con la enfermedad de Alzheimer. Existen diferentes “versiones” (alelos) de este gen. Distintas combinaciones de estas versiones confieren un mayor o menor riesgo de desarrollar la enfermedad. Por ese motivo, además de obtener tu predisposición genética en base a más de 2.000 variantes genéticas asociadas con el riesgo de ser diagnosticado con la enfermedad de Alzheimer, te indicamos tu haplotipo APOE. Es decir, tu “combinación de las posibles versiones de APOE”. El haplotipo APOE está basado en la combinación del genotipo que presentes para dos variantes genéticas muy concretas del gen APOE. Descubre tu haplotipo APOE con ADNTRO.
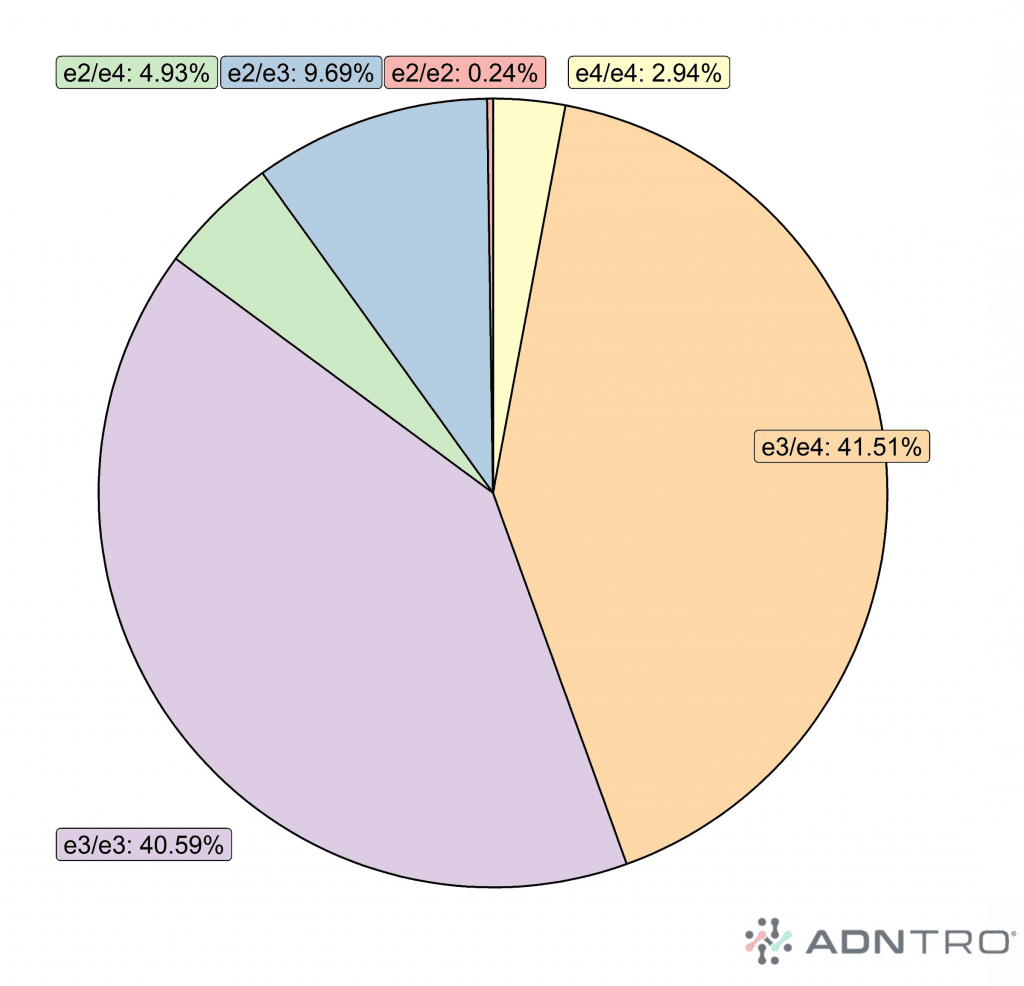
Tu haplotipo APOE
El gen APOE es un gen altamente estudiado y relacionado con la enfermedad de Alzheimer. Dos variantes genéticas comunes dentro de este gen determinan las distintas formas que otorgan un mayor o menor riesgo de desarrollar la enfermedad. Por ejemplo, ser portador de la forma APOE- ε4/APOE- ε4 se ha asociado con un riesgo entre 8 y 10 veces mayor de desarrollar la enfermedad. Heredar la configuración APOE ε4 no significa que vayas a desarrollar la enfermedad, solamente que tienes un mayor riesgo para la misma.
Lo mismo aplica al contrario. El hecho de no tener la configuración APOE ε4, no excluye la posibilidad de desarrollar la enfermedad de Alzheimer. Por ese motivo, tanto el haplotipo APOE como la «barrita» con tu resultado que proporcionamos en ADNTRO son variables independientes que indican si presentas un mayor o menor riesgo a padecer la enfermedad.
El riesgo genético de Alzheimer depende de otras muchas variantes genéticas, siendo el APOE responsable únicamente del 10% del riesgo total.
El haplotipo APOE explica aproximadamente un 10% del riesgo genético explicado por variantes genéticas comunes de padecer la enfermedad de Alzheimer, lo que representa un gran efecto para esta región situada en el cromosoma 19. Se estima que el resto de variantes genéticas comunes de riesgo asociadas a la enfermedad de Alzheimer sean responsables de aproximadamente otro 10% del riesgo genético de la misma, dejando hasta un 80% del riesgo genético de Alzheimer todavía sin descubrir.
Existen tres configuraciones del gen APOE (ε2, ε3, o ε4). ¡Descubre tu haplotipo APOE en ADNTRO!
Fisiopatología del Alzheimer
La primera fase de la enfermedad de Alzheimer se basa en la muerte de las células del hipocampo, región del cerebro donde se almacenan los recuerdos. También se ve afectada la corteza parahipocampal que se encarga de procesos tan importante como la memoria y el aprendizaje perdiendo así la capacidad de almacenar nuevos recuerdos.
Posteriormente, el deterioro se irá expandiendo a otras estructuras cerebrales como la corteza entorrinal que desempeña funciones extraordinariamente importantes como la consolidación de la memoria autobiográfica, aquella que nos permite saber quiénes somos.
La enfermedad de Alzheimer se caracteriza clínicamente por un deterioro cognitivo (pérdida y muerte de neuronas) que interfiere con la independencia en las actividades cotidianas. Y os preguntaréis, ¿qué causa todo este daño en nuestro cerebro? Si hablamos de Alzheimer, a nivel molecular cabe destacar tres grandes características responsables del deterioro cognitivo que caracteriza la enfermedad biológicamente:
- Formación de ovillos neurofibrilares. Estos ovillos aparecen a partir de la proteína tau. Dicha proteína se encarga de estabilizar unas estructuras de nuestro cerebro. El problema viene cuando la proteína tau pierde su actividad estabilizante y forma precipitados (ovillos neurofibrilares), que causa un daño en la estructura de nuestro cerebro.
- Aparición de placas neuríticas. El responsable de la formación de estas placas es una proteína llamada beta- amiloide. Al formarse estos precipitados se desencadena una fuerte respuesta inflamatoria generando así daño en nuestro cerebro. La proteína codificada por el gen APOE es la responsable de romper estas placas de beta – amiloide. Se ha visto que el alelo ε4 es menos efectivo a la hora de realizar esta acción otorgando por tanto un mayor riesgo de padecer la enfermedad de Alzheimer a aquellas personas que lo portan.
- Pérdida de sinapsis funcional. La sinapsis es la forma en la que se comunican nuestras neuronas. Para hacerlo un poco más visual y desarrollar una explicación molecular simple, vamos a imaginarnos una enorme tela de araña creada en la esquina de una pared. Si una hormiga cae en la tela de araña, la estructura permanece intacta, pero en caso de caer un hormiguero entero a la vez, la estructura se rompería, eliminando las conexiones que existían en un primer lugar entre un extremo y otro de la pared. Lo mismo ocurre con nuestro cerebro. Todas las conexiones formadas entre nuestras neuronas (sinapsis) puede verse alterada e incluso destruida con la formación de ovillos neurofibrilares y placas neuríticas que no son más que precipitados (grupos de hormigas) cayendo sobre nuestras conexiones neuronales (tela de araña).
Estudios recientes sugieren que la proteína beta-amiloide no se trata de una proteína anómala, sino de una molécula endógena que forma parte del sistema inmunitario del cerebro. Esto posiciona a la proteína beta-amiloide como elemento clave de la respuesta inmunitaria del cerebro cuando se produce, por ejemplo, un traumatismo cerebral o infección bacteriana.
Debido a la gran similitud entre las moléculas de grasa que componen las membranas de las bacterias y las membranas de las células cerebrales, se postula que la beta-amiloide en los casos de la enfermedad de Alzheimer podría no distinguir entre las bacterias invasoras y las células cerebrales, atacando por error a estas últimas.
En este caso, si la nueva hipótesis es correcta, la enfermedad de Alzheimer se consideraría una enfermedad autoinmune dado que la causa de la enfermedad se debe a un ataque mal dirigido del sistema inmunitario del cerebro.
En ADNTRO seguimos investigando: hacia una predicción más precisa del Alzheimer de inicio tardío
La investigación genómica avanza rápido, y en ADNTRO formamos parte activa de ese avance. Nuestro equipo ha publicado un estudio en la revista científica Genes titulado Development of a k-Nearest Neighbors Model for the Prediction of Late-Onset Alzheimer’s Risk by Combining Polygenic Risk Scores and Phenotypic Variables, en el que desarrollamos un modelo de machine learning capaz de identificar a personas con riesgo de desarrollar Alzheimer de inicio tardío incluso antes de que aparezcan los primeros síntomas.
El modelo combina información genética, la configuración APOE, y variables clínicas fácilmente accesibles como la edad, el colesterol o el historial de diabetes, logrando una sensibilidad del 80% —frente al 63% de modelos comparables anteriores—, lo que supone un avance relevante en la detección temprana de esta enfermedad.
Es importante aclarar que este modelo de investigación, al incorporar datos clínicos y personales, no se ha integrado en la plataforma de ADNTRO, donde trabajamos exclusivamente con información genética por razones de privacidad. En tu perfil, calculamos tu configuración APOE, uno de los marcadores más determinantes en el riesgo de desarrollar Alzheimer, y también relevante para evaluar la respuesta a tratamientos como el lecanemab, recientemente aprobado por la Comisión Europea.
Publicar este tipo de investigación refleja nuestro compromiso con la ciencia: no solo ofrecemos un test genético, sino que contribuimos a construir las herramientas del futuro en medicina predictiva.
Fuentes y enlaces de interés
https://www.fundacioace.com/es
https://www.nia.nih.gov/health/alzheimers-disease-genetics-fact-sheet
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9200312/